前記事では、寒天培地における「デソキシコレート寒天(日本)」と「VRBA(米国)」の違いを通じて、制度ごとに培地設計の意図が異なることを示した。今回はその続編として、液体培地におけるLST培地とBGLB培地の使われ方に注目し、米国(FDAやISO規格)と日本の制度設計の“構造そのものの違い”を見ていきたい。
大腸菌群という検査対象は同じであっても、「どの培地をどの順番でどう使うか」という設計は、制度の背景思想を色濃く反映している。LST → BGLBという二段階構成の米国・ISO方式と、BGLB単独で始める日本方式──この2つの方式を比べることで、なぜ検査の進め方が違うのか、その背景と実務への影響が理解できるはずである。

米国・ISO方式における「LST → BGLB」の合理的な検査設計
ISO規格や米国のFDAの標準法においては、大腸菌群の検査は明確に二段階構成で設計されている(ISO 4831, BAM Chapter 4)。これは、ちょうど“二重の網”を使った漁のような構造である。最初は粗い網(LST培地)で広く拾い上げ、次に細かい網(BGLB培地)で不要なものをふるい落とす──そうすることで、感度と特異性の両立を図る。
まず用いられるのがLST培地(Lauryl Sulfate Tryptose Broth)である。
これは、比較的選択圧の弱い培地であり、グラム陽性菌を緩やかに抑制しつつ、乳糖発酵性の菌を広く拾い上げることができる。言い換えれば、“感度重視”の培地である。
🔬 LST培地の主要成分(代表例)
| 成分 | 濃度例(g/L) | 機能 |
|---|---|---|
| Tryptose | 20.0 | 栄養源 |
| Lactose | 5.0 | 発酵指標(乳糖発酵) |
| Sodium lauryl sulfate | 0.1 | 選択剤:グラム陽性菌阻害 |
| Dipotassium phosphate | 2.75 | 緩衝剤 |
| Potassium dihydrogen phosphate | 2.75 | 緩衝剤 |
| 精製水など | 適量 | 溶媒 |
※上表は主要成分のみを示した簡略版である。実際の処方にはNaCl(食塩)などが含まれる場合があり、メーカーや規格によって若干異なる。実務での使用に際しては各メーカーの製品仕様書または公定書の処方を参照されたい。
その後、このLSTで陽性となったものに対して、BGLB培地(Brilliant Green Lactose Bile Broth)を用いて再確認を行う。BGLBは、胆汁塩とブリリアントグリーンという二重の選択剤により、非標的菌──特に腸球菌などの乳糖発酵性グラム陽性菌を排除する能力に優れている。ブリリアントグリーンもまた、前回紹介した寒天培地VRBA(Violet Red Bile Agar)で用いられるクリスタルバイオレットと同様、自然界には存在しない人工色素である。腸内環境には胆汁酸のような疎水性化合物が存在するため、腸球菌などの一部の菌はそれらに対する耐性を進化的に獲得している。しかし、このような人工的な色素化合物には適応していないため、生育が阻害される。このように、強い選択性を培地にもたらす鍵は、人工合成色素が持つ“異物性”に由来する毒性の活用にある。
🧪 BGLB培地の主要成分(代表例)
| 成分 | 濃度例(g/L) | 機能 |
|---|---|---|
| Peptone(または Tryptose) | 10.0 | 栄養源(アミノ酸・窒素) |
| Lactose | 10.0 | 発酵指標(乳糖発酵) |
| Oxgall / Bile salts | 20.0 | 選択剤:グラム陽性菌阻害(胆汁塩) |
| Brilliant Green | 0.0133 | 選択剤:グラム陽性菌強力阻害(人工色素) |
| Distilled Water | 適量 | 溶媒 |
※上表は主要成分のみを示した簡略版である。実際の処方にはNaCl(食塩)などが含まれる場合があり、メーカーや規格によって若干異なる。実務での使用に際しては各メーカーの製品仕様書または公定書の処方を参照されたい。
このように、「拾い上げる(LST) → ふるいにかける(BGLB)」という二段階構成は、感度と特異性の役割を明確に分離し、偽陰性と偽陽性の両リスクを制度設計上で制御している。
米国・ISO方式のもう一つの特徴──そこで検査が完結する
米国・ISO方式では、液体培地を用いる検査は基本的にMPN法(最確数法)と一体で運用されており、感度と定量性を両立させる仕組みとして制度設計に組み込まれている。
さらに重要なのは、総大腸菌群(coliform)の検査は、このLST → BGLBの検査で“完結する”という点である。MPN法(最確数法)では、この二段階を通じて陽性チューブの本数から定量的な結果を導き出し、そこで最終判定が下される。コロニーを拾い上げて、さらに生化学試験を繰り返すようなフローには進まない。もちろん、大腸菌(E. coli)を特定する場合は追加試験が必要となる。すなわち、「大腸菌群は簡便に、E. coli はもう一段深く」という切り分けが制度側に埋め込まれている。
なぜなら、検査対象は病原菌ではなく指標菌である。本来、指標菌の役割は「衛生状態を手早くざっくり把握すること」であり、迅速性こそが命である。過度の正確性を追求し工程を増やすのは、本質から外れる。制度と設計思想が一致しているからこそ、検査工程もシンプルかつ合理的になっているのである。

※補足:ISOなどの国際基準でも確認試験が規定されている場合はあるが、実務運用では典型反応を重視する傾向があり、日本のように制度上必ず生化学的検査まで踏む運用は一般的ではない。
では日本ではどうか──BGLBでいきなり始める制度構造
一方、日本の制度では、ここで立ち位置が逆転する。たとえば乳製品や魚肉練製品の大腸菌群検査では、最初のステップからBGLB培地を使用してガス発生の有無を判定する構成が採られている(厚生労働省)。つまり、選択圧の強いBGLBを“推定試験”に用いる構造となっている。
ここには一つのリスクが存在する。加熱や乾燥でダメージを受けた“損傷菌”は、強い選択圧のもとでは発育できず、拾い損ねる可能性がある。本来、感度の高い培地で広く拾い、そこから特異性を高める方向に進むのが合理的だが、日本ではいきなり絞り込みから入る構造になっている。

※補足:ただし、例外的に、日本の生食用かきの検査法では、まず乳糖ブイヨン(LB)で推定試験を行い、BGLBを確認試験に用いるフローが採用されている(厚生労働省:生食用かき(成分規格・加工基準・試験法等)。この構造は米国・ISO方式のLST→BGLBに近く、日本の中では例外的に「ゆるく拾ってから絞り込む」設計として運用されている。さらに、他の一般食品と異なり、BGLBでの陽性判定をもって検査が完結するため、迅速な出荷判断が可能となる点でも、米国・ISO方式の合理構造と共通している。
そしてさらに、確認試験が複雑すぎる
しかも、日本方式ではBGLBでガス陽性となった後、EMB寒天での継代接種、典型コロニーの選別、生化学的確認試験(インドール反応、ガス発生など)という、長い確認工程が待っている。日本で確認試験(EMBや生化学試験)が必須となっているのは、日本の食品衛生法における『大腸菌群』の定義が『グラム陰性、無芽胞の桿菌で、乳糖を分解してガスを形成するものの総称』という生物学的な定義に厳格に従おうとしているからである。米国(FDA法)やISO規格のような、『特定の培地で陽性反応が出れば大腸菌群と見なす』という運用(操作的定義)との根本的な違いがここにある。
ここで、「指標菌の検査でここまでやる必要があるのか?」という根本的な疑問が生じる。前回記事(デソキシコレート寒天 vs VRBA)でも同様の構造があった。日本では赤色コロニーをすべて拾い上げて確認試験に進むのに対し、VRBAでは典型的な反応が出れば確認不要とされている。寒天培地と液体培地、違う検査法でありながら、制度設計の背景には共通した“構造の違い”が流れている。

補足:なぜ日本ではこのような複雑な確認工程が制度として定着したのか
背景には、大腸菌群が本来“指標菌にすぎない”にもかかわらず、実務レベルではしばしば病原菌に近い慎重さで扱われてきた歴史がある。その結果、見逃しを極度に恐れる行政的な設計思想が形成され、確認を重ねること自体が“正しい”とされるようになったのかもしれない。本来であれば、指標菌検査とは“ざっくりと衛生状態を示すシグナル”のはずである。それに対して、制度・現場・行政が過剰に「精密診断」を求めてしまった構造的な転倒が起きていると考えられる。
制度の慣性と「検査すべきか」の原点回帰
大腸菌群検査法は、本ブログの別記事もで見たように、EUレベルの主要な微生物規格(Reg. (EC) No 2073/2005 など)では、大腸菌群は基準項目からほぼ姿を消し、多くの場面で大腸菌など別の指標に置き換えられている。実務的には“大腸菌群検査を前提としない制度構造”に移行したと言ってよい。米国でも、特に乳製品分野でcoliformsが制度的な指標として現在も重要な役割を担っている一方、他の食品分野では大腸菌群そのものよりも、大腸菌や別指標へのシフトが進んでいる。したがって、ここで議論されている「培地の使い方」や「培地の選択性の違い」は、あくまで制度的に残っている場面での技術的な話に過ぎない。前回の記事で寒天培地の問題を論じた際にも述べたが、真に問うべきは「そもそも大腸菌群を検査すべきなのか?」という根本的な問いである。
とはいえ、現行の制度の下では、検査担当者が使用する培地の性質や制度的な由来を正しく理解しておくことには実務的な意味がある。特に、国際的な取引先や規格との対話において、検査法に関する最低限の共通認識を持っているかどうかは、現場の信頼性にも直結する。本記事が、そうした「技術としての培地の理解」と、「制度としての検査の妥当性を見直す視点」との両方をつなぐ一助となれば幸いである。

【付録】LST培地に使われる「ドデシル硫酸ナトリウム(SDS)」とは?
LST培地(ラウリル硫酸トリプトース培地)でグラム陽性菌を抑制するために使われる主成分のひとつが「ドデシル硫酸ナトリウム(Sodium Dodecyl Sulfate)」である。これは「ラウリル硫酸ナトリウム(Sodium Lauryl Sulfate)」とも呼ばれ、同じ物質を指す。
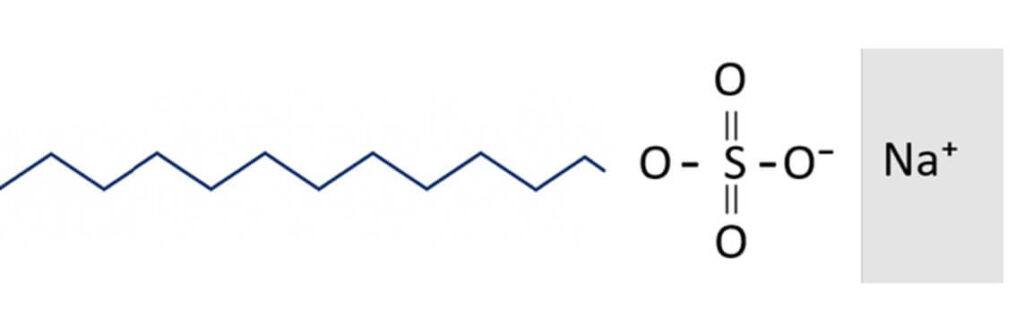
ドデシル(C12)という炭素鎖を持ち、末端が「硫酸基(-OSO3⁻)」となっているのが特徴で、これは一般的な脂肪酸ナトリウム(石鹸)のカルボキシル基(-COO⁻)とは異なる。
炭素数12:界面活性剤の“黄金の長さ”
炭素鎖長は界面活性(疎水性)と水への溶けやすさ(親水性)のバランスに影響し、界面活性剤分野では、炭素数12付近が疎水性と水溶性のバランスに優れるとされることが多く、SLS/SDS(C12)はそのバランスが取りやすい代表例として広く利用されている。鎖が短すぎると疎水性が不足してしまい、細胞膜への作用が弱くなる。一方で、鎖が長すぎると水への溶解度が低下してしまい、まるで重装備すぎて馬から落ちる騎士のように、微生物に到達する前に自滅してしまう。

C12という炭素鎖長は、界面活性力(疎水性)と水への溶解性(親水性)のバランスが非常に優れており、まさに“黄金の長さ”とされている。
硫酸基(-OSO3⁻):完全電離による強い親水性
SDSの末端は、カルボキシル基よりも遥かに強い酸性基である「硫酸基(-OSO3⁻)」である。これは水中でほぼ完全に電離し、強力なマイナスチャージを持つ。この電荷が水分子との相互作用を促進し、界面活性力を高める。
一見すると、「マイナス電荷を持つSDSは、マイナス電荷を持つ微生物表面と反発するのでは?」と思われがちである。確かに、第四級アンモニウム塩のようなカチオン性の殺菌剤は、プラス電荷を帯びており、マイナス電荷の細菌表層と強く結びついて“誘導ミサイル”のように効果を発揮する。しかもそれに加えて疎水性も備えており、まさに“鬼に金棒”である。そのため第四級アンモニウム塩は殺菌剤として強力すぎるため、選択培地としての使用には適さない。
一方、SDSはマイナス電荷を帯びているため、同様の引き寄せ効果は持たない。だが、C12の強力な疎水性相互作用により、電荷の反発を“力でねじ伏せる”ように膜へ突入し、物理的に破壊する。
例えるならば、弓矢で抵抗する兵士に対し、戦車が突っ込んでくるような構図である。

つまり、SDSは第四級アンモニウム塩のような“誘導型”ではなく、“質量アタック型”の選択剤である。誘導はできず、標的に対する親和性はカチオン性には及ばないが、臨界ミセル濃度(CMC)付近での強力な疎水性相互作用によって、微生物の増殖を抑制する程度の阻害効果は十分に持ち合わせている。
SDSは歯磨き粉にも使われている?
なお、このドデシル硫酸ナトリウム(ラウリル硫酸ナトリウム)は、実は市販の歯磨き粉にも広く使われている。あの“泡立ち”の主成分であり、「Sodium Lauryl Sulfate(SLS)」などと表記されている。日常的に目にしているこの成分が、微生物検査の選択培地にも応用されている。