有機酸が微生物を抑える基本メカニズムは、酸性環境下で非解離型(HA)となった有機酸は相対的に脂溶性(疎水性)が高まり、細胞膜を通過して細胞内へ入る。中性に近い細胞内で解離し、水素イオン(H⁺)を放出して内部pHを下げる。その結果、微生物はATPを消費して排出を試みるが負担が大きくなり、増殖が抑えられ、場合によっては死滅する。酢酸ナトリウムの日持ち向上剤であっても、プロピオン酸やソルビン酸のような保存料であっても、基本の作用は同じである。
では、ここで一つ疑問が生まれる。同じメカニズムなのに、なぜ有機酸ごとに効き方が違うのか。 本記事では、この疑問に答えるための要素を解説する。読み終えると、有機酸を使用する際の目安を見積もるための“考え方”が身につくはずである。
有機酸の抗菌性基本メカニズム
まず、有機酸の抗菌性の基本メカニズムについては、本ブログの基礎講座の下記記事で解説しているので、本記事を読む前に確認していただくとよいと思う。
有機酸が微生物を抑える基本メカニズムを解説は下記記事をご覧ください。
基本となる3本柱
さて、同じメカニズムなのに、なぜ有機酸ごとに効き方が違うのか。以下に解説する。
有機酸の抗菌効果は、おおざっぱに言えば「どれだけ“抗菌作用の主役となる状態(HA)”が膜に届き、入った後どう働くか」で決まる。
有機酸の抗菌効果の要素を分けると、次の三本柱になる。
1.pKa
まず酸には「解離型(A⁻)」と「非解離型(HA)」の2つの形がある
酸は水の中で、分子の形のまま(HA)か、水素イオン(H⁺)を放してイオンになった形(A⁻)かのどちらかで存在する。
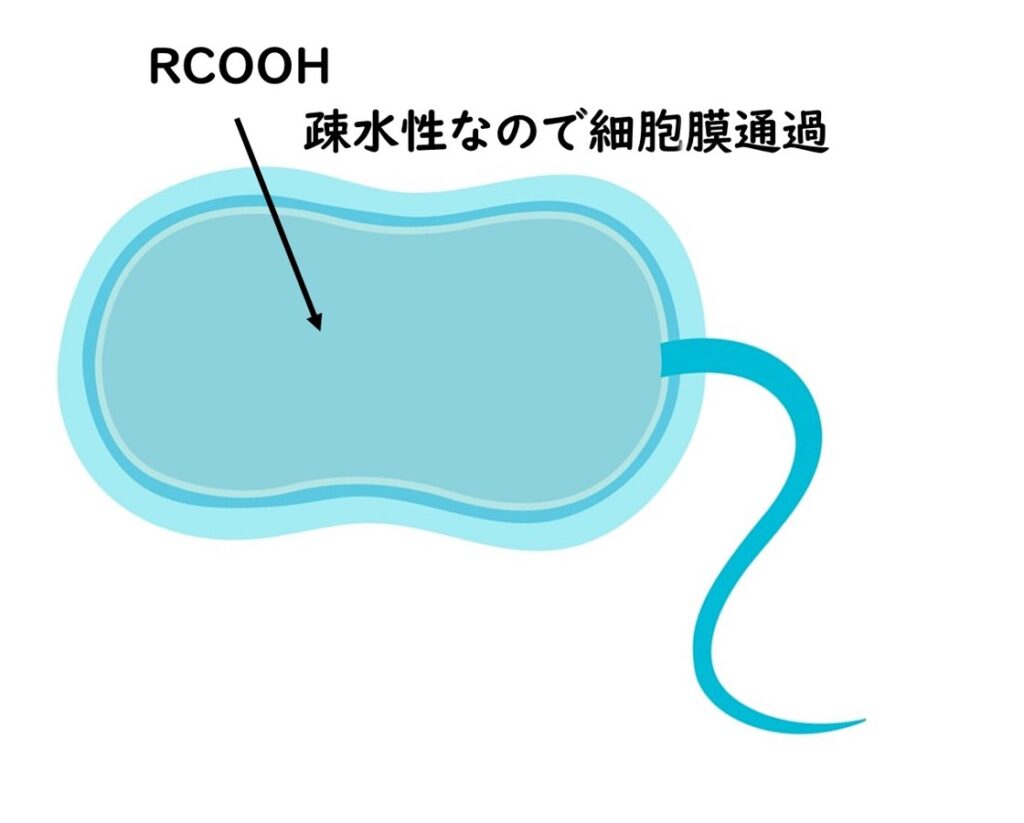
- HA は非解離型で 疎水性(親油性)が相対的に高く、細胞のリン脂質二重膜を通過しやすい。抗菌作用の主役となる形である。
- A⁻ は負電荷を帯びて親水性が高く、膜を通過しにくい。したがって抗菌圧は相対的に小さい。(注:グラム陰性菌では外膜がさらにバリアとなるため、差がより顕著になり得る。)
注:本稿での HA は酸の一般式 H–A を指す。H は酸性プロトン、A は酸から H⁺ が外れたときにアニオン(A⁻)となる部分であり、HAは酸の分子が水素イオン(H⁺)を放していない=非解離型 を意味する。
- H:水素原子(プロトン)
- A:酸の残りの部分(アニオンになる部分)
- 例)酢酸の場合
- 非解離型:CH₃COOH(これが HA)
- 解離型:CH₃COO⁻(これが A⁻)+ H⁺
つまり「HA」は化学の一般記法で、有機酸の非解離の状態=膜を通りやすい“中性の姿”、すなわち抗菌作用の主役となる酸の形を表す。
そして、pKa は、酸が水の中でどのくらい解離しやすいかを示す数字であり、「酸分子の半分が非解離型、半分が解離型になる pH」 を意味する。例えば酢酸ならpKa=4.76。つまりpHが4.76のとき、HAとA⁻は1:1
pKaの影響の具体例(酢酸 vs 乳酸)
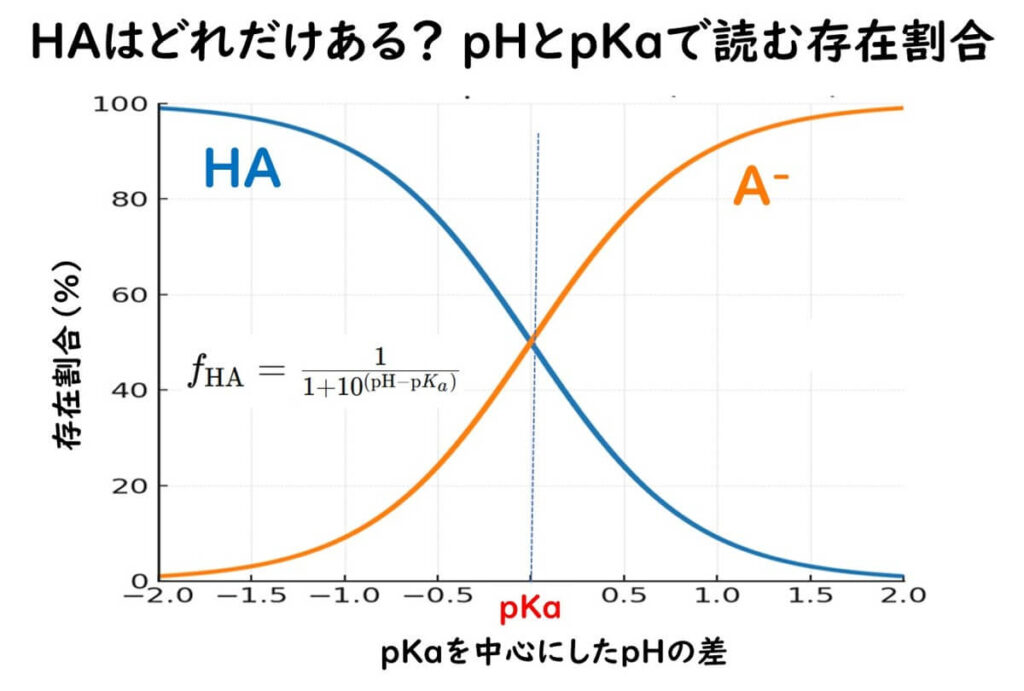
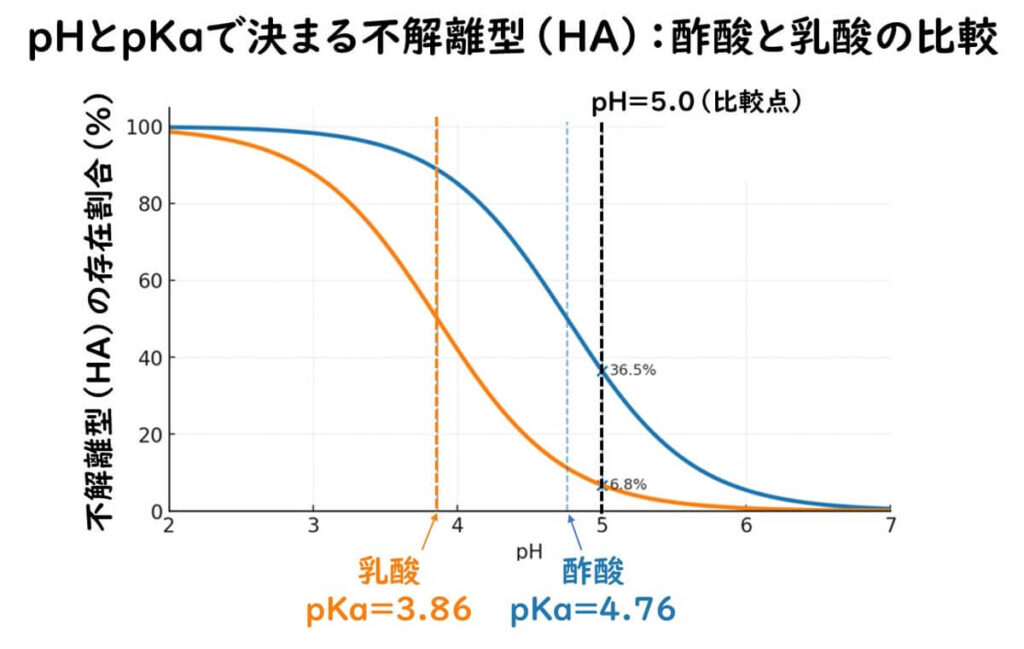
たとえば、酢酸の pKa は 4.76、乳酸は 3.86(25℃代表値)である。pH=5.0 の食品を想定すると、
- 酢酸では、わずかにpKaよりアルカリ側なので、“効く形(HA)”の割合は 約36%となる。
- 乳酸ではpKaより1以上アルカリ側なので、“効く形(HA)”は約7%と少なくなる。
同じ総酸量なら、酢酸の方が“効く形(HA)”がはるかに多く、弱酸としての抗菌性は強いと見積もれる。
ただし、これはpKaレバーだけを見た一次近似である。後述のとおり、疎水性(膜分配)やアニオン固有作用、さらに塩型の浸透圧・aw低下、標的微生物の外膜・代謝などの影響で差が縮む/逆転することもある。
※1: pKaの違いはどこから来るのかについて理解したい方は、本記事の末尾に解説しておいたので、化学に興味のある方はご覧ください
※2: pKaからpHが1上昇したり、下降したりした場合の、“効く形(HA)”の割合の計算方法について、理解したい方は、本記事の末尾に解説しておいたので、化学に興味のある方はご覧ください
酸型と塩型(Na/K/Ca塩)は何が違うのか
ここで、読者の中には、酢酸やプロピオン酸ではなく、酢酸ナトリウムやプロピオン酸カリウムなどの「塩はどうなの?」という疑問が生じるかもしれない。
結論から述べれば、効力を左右する本質は pH と pKa が決める “HA(非解離型)” の割合である。最終 pH が同じなら、酸型を入れても塩型を入れても HA:A⁻ の比は熱力学的に同一に決まる。ゆえに「酸型か塩型か」そのものより、製品pHと酸種(pKa)が支配的である。
※ ただし実務では、酸型はpHを下げやすく、塩はわずかに上げがちであり、溶解性・当量(例:プロピオン酸Caは二価)・官能の違いもある。したがって、選定は最終pHを先に設計した上で、扱いやすさ(溶解・味・設備)で決めるのがよい。

2.疎水性(膜に届く“運びの良さ”)
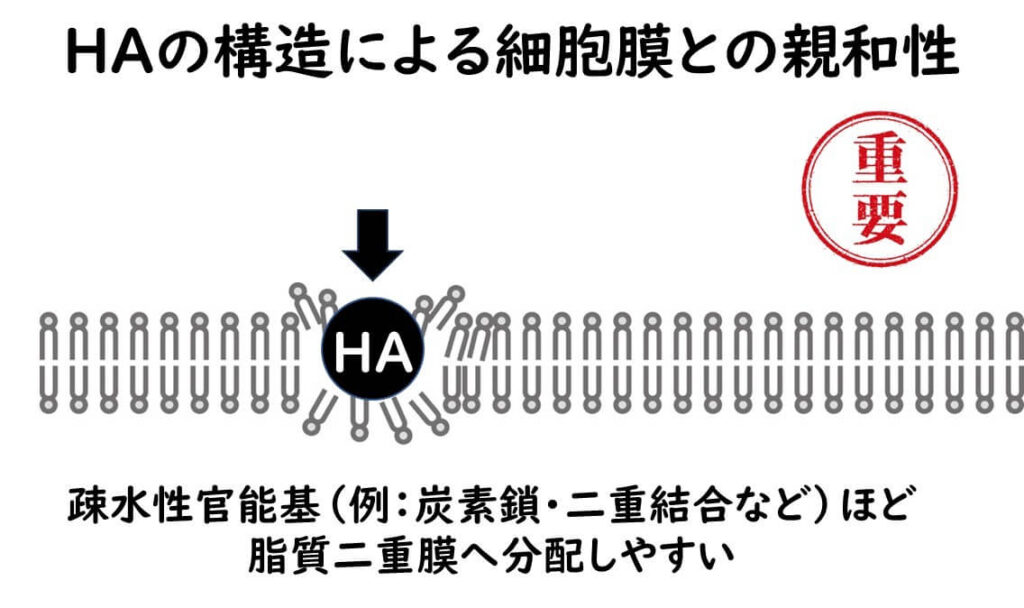
- HA の量だけではなく、HAの構造による細胞膜との親和性も重要だ。
- 疎水性官能基(炭素鎖や二重結合など)が大きいほど、膜の脂質層に溶け込みやすくなる傾向がある。
- ただし、疎水性が強すぎると水層に溶けにくくなり、逆に効率が落ちる場合もある。
疎水性効果の具体例
酵母・カビ
酢酸(C2)とプロピオン酸(C3)は炭素が1つ違うだけである。炭素数が増えると疎水性が上がり、未解離型(HA)が原形質膜に分配・透過しやすくなる。さらに pKa も 4.76→4.87 とわずかに高くなるため、同じpHなら“効く形(HA)の母数”も少し増える。その結果、酵母・カビ(酸性域)では一般にプロピオン酸の方が防カビ力が強く出やすい。
例えば、糸状菌(カビ)に対して、同条件でプロピオン酸の方が酢酸より低いMIC(=強い)を示す系統的データがある(Dagnasら、2015)。論文では、C3 は C2 より疎水性が高く、さらに pKa もわずかに高いため、同じpHなら“効く形(HA)の母数”もわずかに多い——この2要因の積として説明されている。
細菌
細菌に対しては、アニオン側の疎水性の度合い(炭素数の数)単純化できない。特にグラム陰性は外膜が、疎水性物質のバリアとして作用する部分もあり、「鎖長が長いほど常に強い」とは言い切れない。一方、グラム陽性菌には外膜がないため、未解離型の疎水性が効きやすい場面はある。しかし細菌では代謝や酸耐性応答の影響が大きく、C3(プロピオン酸)>C2(酢酸)が常に成り立つわけではない。
3.アニオン固有作用(中に入った後の“第2の刃”)
- HA が膜を通って細胞内で解離すると、アニオン(A⁻)が残る。
- このアニオンが、微生物の代謝や呼吸系を邪魔する作用を持つことがある。
- 例:プロピオン酸は糸状菌で代謝経路を詰まらせる(Brockら、2004)。ソルビン酸は酵母で呼吸回路を阻害する(Stratfordら、2020)。
酸種によって作用の種類や強さが違うが、まだ完全には解明されていない部分も多い。
結論:実務へのヒント
本稿は、有機酸を食品の保存料として使用する際、原理の理解なしに保存試験を行わないために、基本的な有機酸の抗菌作用の原理を整理したものである。
ただし、ここで述べたのはあくまでも考え方の整理であり、理論だけで有機酸の種類や配合量が自動的に決まるわけではない。食品マトリックス(油脂、糖、タンパク質など)の存在や対象微生物の性質による影響も大きいため、最終的には保存試験を行い、実際の製品条件下で確認することが不可欠である。
しかし、その試験を効率よく設計し、結果を正しく解釈するためには、有機酸の作用原理の理解が不可欠である。

参考:
🤵♂️pKaの違いはどこから来るのか(化学に興味のある方へ)
pKaの違いの理由については化学の専門領域であり、本稿の目的(酸の選定と設計)には不要である。この注意書きセクションは読み飛ばしていただいて構わないが、化学的側面に興味のある方向けに、簡単に説明しておく。
✅アニオン(A⁻)が安定になるほど、酸はH⁺を手放しやすくなり、pKaは下がる
アニオン(A⁻)が安定化に与える要素
1️⃣誘起効果(−I):カルボキシルのすぐ隣に電気陰性原子(O、Cl など)や=Oがあると、電子を引っ張ってA⁻を安定化 → pKa↓。
2️⃣共鳴分散(−M):二重結合や芳香環に共役して電荷が分散できると pKa↓。
3️⃣ 距離効果:この影響は近いほど強く、1炭素離れるごとに弱くなる。
4️⃣逆向き(+I/供与性):アルキルのように電子を押し出す基は A⁻を不安定化 → pKa↑。
✏️食品での身近な例
- 乳酸(pKa≈3.86)< 酢酸(pKa≈4.76):乳酸はα位の–OH が強い −I を与えるため、A⁻がより安定 → pKaが低い。
- 安息香酸(pKa≈4.20)< 酢酸(pKa≈4.76):芳香環に共鳴で電荷が分散 → pKaが低い。
(同じ飽和脂肪酸の酢酸(C2)とプロピオン酸(C3)は構造が近く、pKaは4.76 と 4.87で差が小さいのもこの理屈に合う。)
🤵♂️pKaからPHが上下した場合の“効く形(HA)”の割合の計算方法
pKaからPHが上下した場合の“効く形(HA)”の割合(fHa)は、下式(ヘンダーソン–ハッセルバルヒ式)から求めることができる。
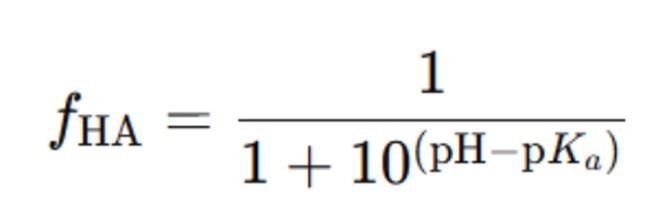
たとえば、酢酸を例に取って考えてみよう。酢酸の場合pKa≈4.76である。今、pH=pKa、すなわち4.76である場合、pKaの定義から、fHa=0.5(50%)となるはずである。代入してみよう。
fHA=1/[1+10(4.76-4.76)]=1/(1+100)=1/(1+1)=1/2=0.5
定義通り、50%となった。
では、次にpHがpKaより1高い(すなわちpH=5.76)だった場合、どうなるか?
fHA=1/[1+10(5.76-4.76)]=1/(1+101)=1/(1+10)=1/11
≈9.09%となる。
では、次にpHがpKaより1低い(すなわちpH=3.76)だった場合、どうなるか?
fHA=1/[1+10(3.76-4.76)]=1/(1+10-1)=1/(1+0.1)=1/1.1
≈90.91%となる。