大根には殺菌効果があるとよく言われる。その理由は、大根に含まれる イソチオシアネート という成分の抗菌作用にある。ところが最近、ノロウイルスに汚染された「殺菌効果のあるはずの大根おろし」による食中毒が発生した。「大根には殺菌効果があるはずなのに、なぜウイルスに効かなかったのか?」——本稿では、この疑問に対して ウイルスと細菌の構造的な違い という観点から分かりやすく解説する。
最新ニュース:大根おろしが原因とみられる大規模食中毒
2025年9月(報道は10月)、愛知県あま市の食品加工会社が製造した大根おろしを原因とする大規模な食中毒事件が発生した。居酒屋や焼肉店など複数店舗で259人が下痢や嘔吐などの症状を訴え、このうち113人からノロウイルスが検出されたと複数の報道機関が伝えている(情報源:複数の報道機関、2025年10月)。
ネット上では「大根には殺菌作用があるはずでは?」といった声も上がった。確かに、大根には殺菌作用を持つイソチオシアネートという成分が含まれている。
では、なぜ殺菌作用のある大根でノロウイルス食中毒が起きたのか?

大根に含まれる殺菌成分 ― イソチオシアネート(ITC)の作用機序
イソチオシアネートの構造と反応性
イソチオシアネート(ITC)は、アブラナ科植物由来の辛味成分であり、同時に強い抗菌活性をもつ化合物である。
分子構造の基本骨格は以下の通りである:
R−N=C=S
- 「–N=C=S(イソチオシアネート基)」部分は非常に反応性が高く、殺菌活性の主要因となる。
- 一方、「R基」の種類によって分子全体の性質が変化する。
特に アリル基(–CH₂–CH=CH₂) のような疎水性R基を持つ場合、脂質膜に対する親和性が高くなり、これが殺菌作用の第1段階を決定する。
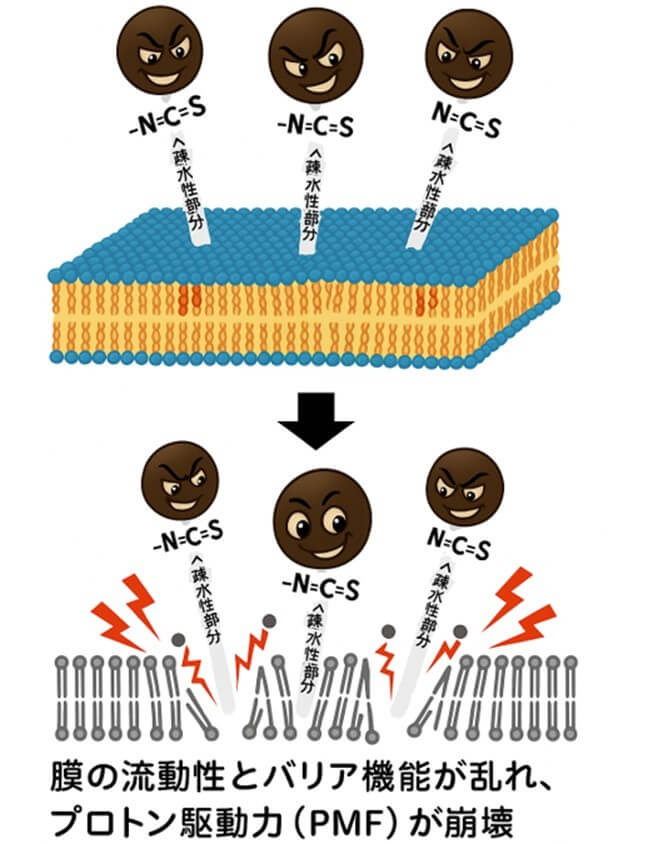
1.細胞膜を破壊する
- AITCは疎水性のアリル基(R基)を持つため、細胞膜の脂質二重層に容易に侵入する。
- その結果、膜の流動性とバリア機能が乱れ、プロトン駆動力(PMF)が崩壊する。
- 物質漏出とエネルギー喪失により、細菌は短時間で死滅する。
👉 ここで重要なのは、膜に作用できるのは細菌が脂質膜を持つからである。R基が疎水性であることが、この作用を可能にしている。
2.酵素のチオール基(–SH)と反応し、活性を失わせる
- イソチオシアネート基(–N=C=S)は求電子性を持ち、酵素中の システイン残基の–SH と求核反応を起こす。
- このとき、チオウレア結合が形成され、酵素の活性部位がブロックされる。
- 解糖系・呼吸鎖・脂肪酸合成といった生命活動の基幹酵素が失活し、代謝が停止する。
👉 この“酵素スイッチの破壊”がITCの抗菌作用の中核。
ただし、このように書いても、化学を深く専門としている読者は別として、多くの読者は、今ひとつピンとこないかもしれない。そこで、もう少し、噛み砕いて解説してみたい。
「求電子性」とは「電子が欲しくて仕方がない性質」
イソチオシアネート基(–N=C=S)は、電子を強く引き寄せようとする性質(求電子性)を持っている。これは、たとえるなら「電子が欲しくてウズウズしている磁石」のような状態だ。
もう少し化学的に言うと、炭素(C)が電子を引き寄せやすい窒素(N)と硫黄(S)の間にあり、両側に電子を引っ張られてしまうため、Cの周りは“電子スカスカ”になる。たとえ話でいえば、Cは「ちょっとずるい友達(NとS)」に両脇を固められて、お財布(電子)をスルスル取られてしまう状態。つまり「金欠なんだけど!」と叫んでいるのと同じで、これが求電子性が高いということだ。

高校化学的に言えば、Cは部分的に正(δ⁺)に帯電しており、電子を引き寄せたがる状態にある。
一方、チオール基(–SH)は「電子を持っていて反応しやすい」
一方、酵素中の システイン残基のチオール基(–SH)は、硫黄原子が電子を持っている“お金持ち”のような状態だ。硫黄(S)は酸素(O)よりも原子が大きく、電子を外側にゆるく握っているため、他の分子に電子を“渡しやすい”性質を持っている。たとえるなら、お金をお尻のポケットにルーズに突っ込んで歩いている人のようなものだ。だから、必要があればすぐにお金(電子)を渡せるし(=反応性が高い)、その裏返しで、泥棒(求電子剤)にもすぐ奪われてしまう。
これが、チオール基の反応性が高い理由である。

「電子を欲しがる磁石」と「電子を持つお金持ち」が出会うと?
電子を強く引き寄せる性質をもつイソチオシアネートと、電子を供与する –SH 基が出会うと、–SH 側が求核剤となり、イソチオシアネートの炭素を攻撃する。この反応によって、S-チオカルバメート結合が形成される。
このとき形成される化学構造は下図のように、イソチオシアネート基(–N=C=S)の炭素に –SH が付加し、S-チオカルバメート型の共有結合を作る
R–S–C(=S)–NH–R′
この反応によって、酵素の活性部位に存在するシステイン残基の –SH 基が不可逆的に塞がれてしまう。これは、酵素にとって「スイッチを押されて OFF になる」ことと同義である。すなわち、酵素の側が自らイソチオシアネートに反応し、その結果として自分自身の活性を失う構図である。
※たとえ話ではイソチオシアネートが酵素を「狙って攻撃」するように描いているが、実際には酵素の–SH基が自ら反応し、イソチオシアネートという“罠”にかかる形で活性中心が塞がれる。

酵素スイッチがOFFになると何が起こるか
酵素は、解糖系や呼吸鎖など生命活動の根幹を支える装置。
このスイッチが壊れると、
- 代謝が止まる
- エネルギーが作れなくなる
- 細菌は死んでしまう
👉 つまり、ITCの殺菌の核心は「酵素のスイッチOFF」にある。
※上記2作用機序以外にも、酸化ストレス誘導やバイオフィルム阻害といった副次的作用も知られているが、実際の抗菌効果を支える主要因はこの①と②である。
ノロウイルスに対する実験的な効果の検証― 限定的な抗ウイルス効果
近年、イソチオシアネートの感染価減衰効果については複数の研究が行われている。特にノロウイルス感染症に関連しては、Murine Norovirus(MNV)およびヒトノロウイルスを対象とした実験で、AITC(アリルイソチオシアネート)が濃度・温度・処理時間依存的な感染価減衰を示すことが報告されている。高濃度(0.5%)かつ37 ℃で一晩処理した条件では、MNVに対して約3.75 log TCID₅₀/mLの感染価減衰が認められた。
一方、食品への実用的な処理時間(15〜30分)では統計的に有意な感染価の減衰は認められていない。この実験結果から、AITCによる効果は長時間・高温条件に強く依存していることが明らかである。
さらに、これらの実験条件は実際の食品サービスや加工環境を反映していない。例えば大根おろしは常温または冷蔵状態で生食されるため、高温・長時間処理のような条件は現場では想定しにくい。低温または短時間曝露によるウイルス不活化はごくわずかであり、実用上は無視できるレベルと考えられる。
AITCは特定の条件下では高い感染価減衰効果を示す可能性があるものの、実用的な短時間処理では効果が限定的であり、これは開放環境下におけるAITCの高い揮発性にも起因していると考えられる。したがって、現実的な処理条件下ではノロウイルスはITCに対して基本的に耐性が高いといえる(Falcó & Sánchez, 2024)。
ウイルスの構造とITCが効かない理由ーウイルス構造との関係
ここで、まずウイルスの基本的な構造を整理しておく
ウイルスには大きく分けて 2種類 がある。
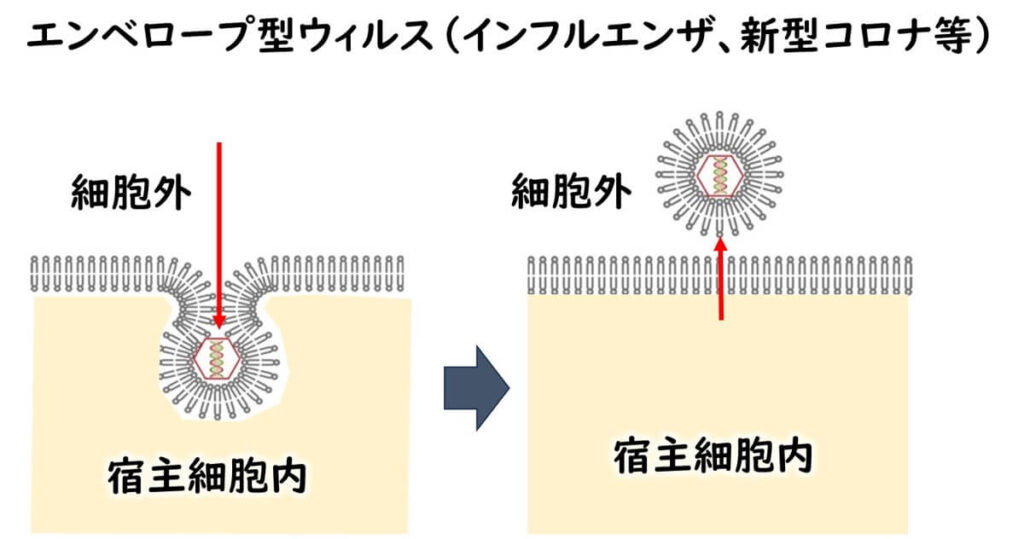
1️⃣エンベロープ型:脂質膜で覆われている(例:インフルエンザウイルス)
2️⃣ノンエンベロープ型:脂質膜がない(例:ノロウイルス)
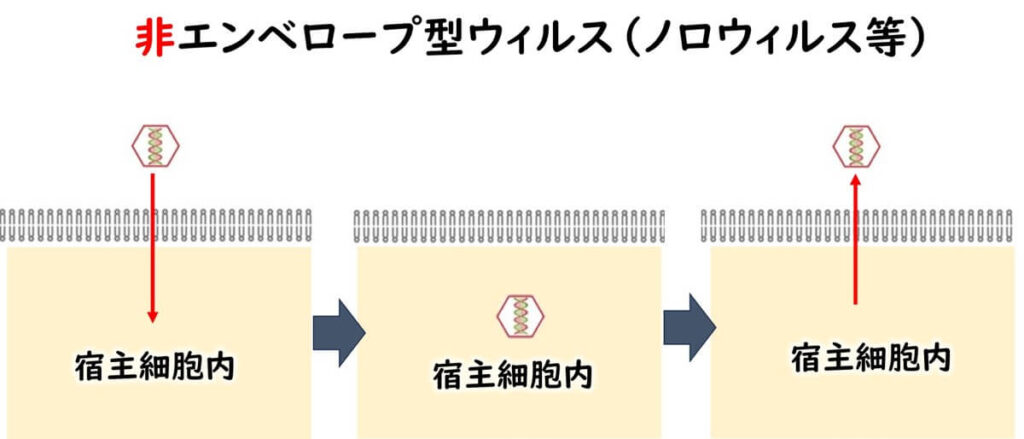
ノロウイルスは ノンエンベロープ型 に分類される。
つまり、細菌とは構造がまったく異なり、ITCの攻撃が効かない理由が明確にある
ノロウイルスには「脂質膜」がない
ITCの代表的な作用である「膜の破壊」は、膜そのものがないウイルスには成立しない。細菌のように膜を攻撃して失活させることができないのだ。
キャプシドは「構造タンパク」であり、チオール修飾の標的ではない
ノロウイルスは外側を キャプシド と呼ばれるタンパク質の殻で覆っている。しかしこのキャプシドは、細菌のような「代謝酵素」ではなく、構造を支えるためのタンパク質である。
さらに
- キャプシド表面にはITCが反応する“遊離チオール基”がほとんどない注)
- 多くはジスルフィド結合(–S–S–)で安定化している
そのため、ITCが攻撃する“スイッチ”自体が存在しない。
高濃度・長時間接触ではごくわずかに影響を与える報告もあるが、実用レベルでは不活化できない。
注
キャプシドタンパクにもシステイン残基は存在するが、立体構造内に埋もれており、表面に–SH基が露出していないため、ITCとの反応は起こりにくい。

ではエンベロープ型のインフルエンザウイルスには効くのか?
一方、インフルエンザウイルスは脂質膜(エンベロープ)を持ち、ITCによる高い抗ウイルス活性が in vitro 実験で示されており、この膜タンパク質の機能を阻害する(または付着・融合プロセスに干渉する)ことで感染を防ぐ可能性が示唆されている(Li et al., 2019; Cho et al., 2022)
ただし、ここで注意が必要である👇
- これらの研究は 食品汚染を想定したものではなく
- スルフォラファンなどのITC類を摂取することで 感染予防や免疫応答強化に寄与する可能性 を評価したものである。
まとめ ― ノロウイルスには「標的」がない
| 対象 | 膜破壊 | 酵素/タンパク質修飾 | 実用的効果 |
| 細菌 | 有効(膜透過性増大) | 酵素活性阻害 | 顕著 |
| ノロウイルス(ノンエンベロープ) | 構造上作用せず | 標的なし(酵素非存在) | 無効 |
| インフルエンザウイルス(エンベロープ) | ミクロ的には影響あり | 膜タンパク機能阻害の可能性 | 食品汚染対策としては無効 |
ITCは細菌には強い効果を示すが、ノロウイルスには「標的」がなく、構造的に効かない。
インフルエンザの場合も、直接的な食品汚染対策ではなく 免疫応答強化という別の文脈 になる。
おわりに
今回の記事では、イソチオシアネート(ITC)がノロウイルスには効果を示さない理由について解説した。これはウイルスと細菌の構造的な違いに起因するものであり、ノロウイルスには脂質膜も酵素タンパクも存在しないため、ITCの“攻撃”が届かないのである。
一方で、イソチオシアネートはこれまでにも多くの研究で、細菌に対する抗菌作用が報告されており、食品中の自然由来の抗菌成分として注目されている。特に、細菌の細胞膜や酵素に直接作用することで、生育を抑制することができる。
つまり、ITCは細菌の制御には有効である一方で、今回のようなノロウイルスには効果を発揮しない。。ノロウイルスはITCを含む多くの天然抗菌化合物に対して耐性を示すため、厳格な手洗い、器具の消毒、感染した食品取扱者の排除といった予防的衛生対策が、ノロウイルス対策の基盤であり続けている。食品衛生の現場では、この違いを正しく理解した上で、目的に応じた衛生管理手段を選ぶことが極めて重要である。


