日本における食品安全規制では、糞便系大腸菌群(E.coli、ブロック体)の検査に関する規格基準が設定されている。以前、サイエンスフォーラムで実施した食品微生物学入門講座の受講生と個別質疑を行っている際に、この会社の日常的な自主検査において、糞便系大腸菌群の検査(E.coli、ブロック体)から、β-グルクロニダーゼ活性を用いた酵素基質培地に切り替えたいと上司に話したところ、この培地では、大腸菌O157:H7がカバーできていないのでダメだと言われたという経験を私に話されたことがある。この記事では、本当にそうなのか?このような理解の仕方が見落としている盲点について解説し、また、改めて、指標菌培地としての酵素基質培地の役割を整理してみたい。

β-グルクロニダーゼを用いた酵素基質培地の原理
β-グルクロニダーゼを用いた酵素基質培地での大腸菌検出は、大腸菌が有する特有の酵素活性に基づいている。β-グルクロニダーゼ (β-glucuronidase) は D-グルクロン酸のβ型配糖体に作用してそのグルクロニド結合を加水分解し、グルクロン酸を生成する酵素である。
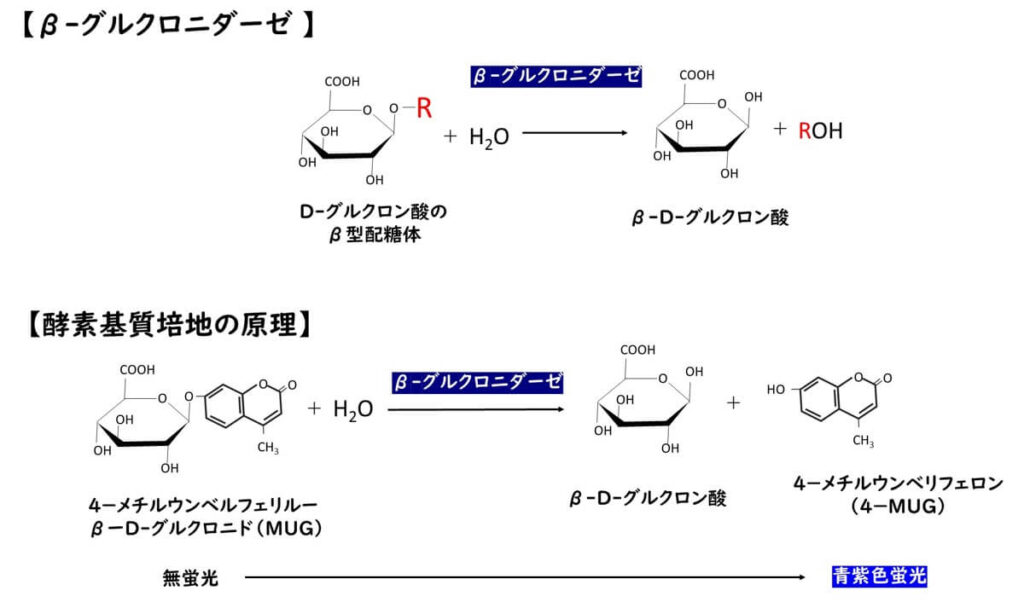
この際、特定の発色基質がこの酵素の存在下で分解されると、色の変化や蛍光を発する。
β-グルクロニダーゼに対する発色酵素基質として、MUG(4-メチルウンベリフェニル-β-D-グルクロ二ド)とX-グルクロ二ド(5-ブロモ-4-クロロ-3-インドリル-β-D-グルクロニド)などがある。大腸菌細胞は、これらのの化合物を完全なまま吸収でき、細胞内のグルクロニダーゼがこれらの化合物のグルクロニド結合を切断する。その結果生成されたMUGは長波長の紫外線下で蛍光を発し、X-グルクロニダーゼは青色に発色する。すなわち、大腸菌コロニーが持つβ-グルクロニダーゼ反応後の色の変化や蛍光を視覚的に観察することで、大腸菌の存在や数を間接的に検出することができる。この原理に基づき、各種の培地が考案されている。
なお、β-グルクロニダーゼ活性は、グラム陰性菌では大腸菌(Escherichia coli)の大部分(90~96%)が保有している(Thompson et al.,1990、Hansen et al.,1984)。その他、赤痢菌、エルシニア菌、サルモネラ菌の一部も本酵素活性を持っている場合があるが、原則として大腸菌のみが産生し、他の腸内細菌科菌群がそれに陽性を示すのは稀である。例えば、Thompson et al.,1990は、大腸菌以外の菌について、ヒト臨床検体から分離された421株のグルクロニダーゼ活性を調べ、サルモネラ92株中MUG陽性は3株のみ、赤痢菌については、Shigella sonneiの分離株14株中11株、Shigella boydiiの分離株5株中1株、Shigella flexneriの分離株17株中1株のみがMUG陽性、さらに、エルシニア・エンテロコリティカは12株中陽性株は見当たらなかったと報告している。
酵素基質培地でもO157:H7以外のSTECは検出可能
上述したように、β-グルクロニダーゼ活性は、病原性、非病原性を問わず、大腸菌の90~96%が持っていることが分かっている。そのなかで、血清型 O157:H7クローンはまれな例外と位置付けられている。
殆どのO157:H7がβ-グルクロニダーゼ活性をもっていないメカニズムとしては、O157:H7は、O55:H7 (β-グルクロニダーゼ活陽性)を祖先として、段階的にソルビトール発酵および β-グルクロニダーゼ活性を失ったと考えられている(Wick et al., 2005)。O55:H7のβ-グルクロニダーゼ遺伝子のフレームシフト変異が起きたために、この酵素を発現できなくなったと考えられている。つまり、 β-グルクロニダーゼ活性の喪失の経緯から見ると、この喪失は、O157:H7特有の進化的遺伝子変異で起きた現象といえる。
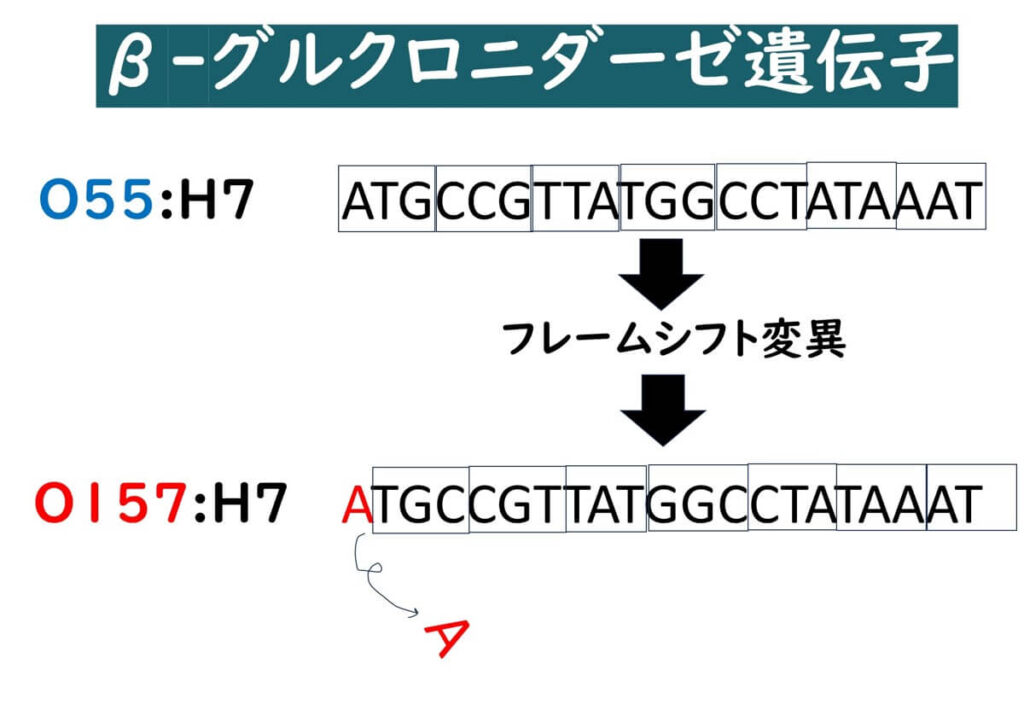
このように、β-グルクロニダーゼを持っていないのは、一般的に言えば腸管出血性大腸菌の中でもO157:H7のみであると整理できる。
しかし、他の血清型の腸管出血性大腸菌がβ-グルクロニダーゼ陽性であるかどうかについては、O157:H7ほどβ-グルクロニダーゼ活性との関連が研究されていないため、O157:H7のようにβ-グルクロニダーゼ活性の有無については現時点では明確に断言できない部分がある。実際、他の血清型でもO157:H7と同様にβ-グルクロニダーゼ活性を失う進化経路が存在する可能性も考えられ、現時点ではまだ充分に研究が行われていないと言える。
その中で、β-グルクロニダーゼ活性陽性例のいくつかの事例を紹介すると、次のようになる。
- 2014 年 7 月、イギリスで志賀毒素産生大腸菌( STEC) O55:H7 が発生し、31 人の患者が発生し、そのうち 13 人 (42%) が溶血性尿毒症症候群であった。この腸管出血性大腸菌はβ-グルクロニダーゼが陽性であると報告されている(Schutz et al, 2017)。
- 米国とカナダで発生した小麦粉に関連した志賀毒素産生大腸菌 O121:H19 の 49 株のβ-グルクロニダーゼ活性も測定した結果、6株を除くすべての株は、正常な β-グルクロニダーゼ活性を示した(Gill et al.,2022)。
- O157:H7以外の血清型の志賀毒素産生大腸菌株(O1:H-、0111:H8、0111:H-、0113:H21、026:K60、091:H21、0121:Hl9、0145:H-、および型別不能株)を検査したところ、β-グルクロニダーゼ反応は、陽性から陰性まで、様々であった(Krishnan et al.,1987)
- チリの牛からの STEC 分離株の研究では、合計 93 の異なる血清型O157:H7以外の志賀毒素産生大腸菌( STEC)についてβ-グルクロニダーゼ活性 を調べた結果、96.8%(90/93) が陽性であったと報告されている(Diaz et al., 2021)。
一方、O157:H7以外の血清型でも、β-グルクロニダーゼ活性陰性の報告も存在する。
- 2012年の日本の山口県で4歳女児の腸管出血性大腸菌食中毒に関連して牛から分離された志賀毒素産生大腸菌( STEC)O26はβ-グルクロニダーゼが陰性であると報告されている(Kameyama et al.,2013)
このように、その他の血清型の腸管出血性大腸菌については、基本的にはβ-グルクロニダーゼ活性陽性株が多いものの、中には陰性株も存在していると整理できそうだ(現時点でのデータ)。

いずれにせよ、β-グルクロニダーゼを利用した酵素基質培地で検出できないと結論づけられているのは、あくまでも血清型O157に限定された話であり、その他の腸管出血性大腸菌が検出されないわけではないことをまず理解しておく必要がある。
糞便系大腸菌群検査でもO157:H7の一部は検出できない
実は、大腸菌O157:H7が検出できないのは酵素基質培地だけでない。糞便系大腸菌検査(44.5℃)でも、大腸菌O157:H7の株の中には検出できない株が存在することがある。国際標準規格ISO 16649-1:2018では、大腸菌の検出における培養温度を44°Cに設定しているが、44°Cの培養温度では大腸菌0157:H7の株の中には、ほとんど増殖できないものが存在する(ISO 16649-1:201)。
食品会社の自主検査において、糞便系大腸菌培地検査から酵素基質培地に切り替えようとした場合、O157:H7の検出ができていないということが酵素基質培地メーカーのマニュアルに必ず記載されているため、培地の変更に躊躇する事態が生まれるようである(前述の私への相談者の上司の例)。しかし、44.5℃の培養温度に依存している糞便系大腸菌検査でも必ずしもすべての大腸菌O157:H7が検出できているわけではない事実を認識すれば、「酵素基質培地では、大腸菌O157:H7がカバーできていないので、糞便系大腸菌検査(44.5℃)に比べてダメ」という理解が正確でないことに気づくと思う。

そもそも、指標菌としての大腸菌検査では、O157:H7の検出を目指していない
最も重要な理解として、そもそも、指標菌としての大腸菌検査においては、そもそもO157:H7の検出を目指していない。簡単な事実であるが、実は、このことは食品会社の多くの品質管理担当者が間違えやすいポイントだ。そもそも大腸菌の検査は何のために行っているかとことについて、今一度、考えてみよう
指標菌とは何か?指標菌とは、その菌が検出されたら、その菌と同じような環境的挙動を共にしている病原菌が存在している可能性が高いと推測することである。つまり、その培地そのものにで検出される菌と、そこから推測する病原菌とは異なるのが大前提である。
また、次の点も多くの品質管理者が見落としやすいポイントである。
例えば大腸菌O157:H7など、分布量の少ない病原菌の汚染リスクを、少ないサンプル数で検査を行って、正しくリスクを判定することは至難の業だ。もし菌の汚染率が1%であれば、1サンプルを分析した場合、99%の確率で汚染を見落とす(偽陰性)。たとえ、30サンプルを分析しても、74%の確率で汚染を見落とす(偽陰性)。95%の精度で汚染を見落とさないためには、298サンプルの分析が必要である。サンプル数と精度については下記入門記事をご覧いただきたい。

したがって、このように標的病原菌の分布が少ない場合には、数少ないサンプルを分析しても検査の意味がそもそもないということになる。そこで、もう少し分布確率の高い細菌、即ち大腸菌などの指標菌を検出するわけだ。指標菌検出であっても、やはり上述のサンプル数と偽陰性率の問題は残るが、病原菌そのものの検出よりは分布率が高いので(したがって偽陰性率が低い)、指標菌を用いているわけである。
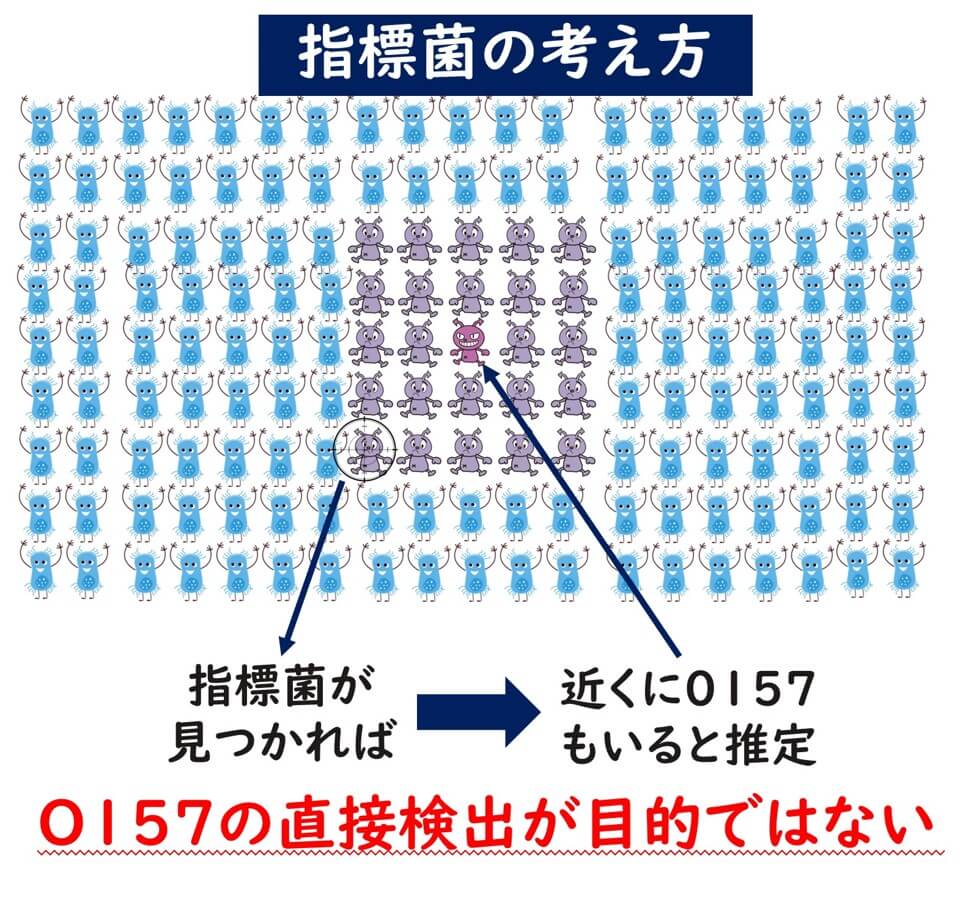
以上のように、指標菌検査の意味をまず理解する必要がある。従って、指標菌としての大腸菌検査の酵素基質培地の平板上で大腸菌O157:H7が検出できないとしても、そもそも、指標菌検査では病原菌を寒天培地上で検出することを目的としていない。この点が、これまで私に相談された品質管理者の多くが、時に混乱し、間違えやすいポイントのようである。
まとめ
この記事は、酵素基質培地を使用した大腸菌検査における指標菌としての意義を再度理解していただくために執筆した。特に、冒頭で述べたように、酵素基質培地は大腸菌O157:H7を検出するのに適していないため、品質管理担当者がその使用に躊躇することがある。この記事が品質管理担当者の誤解を解消し、酵素基質培地の利用に役立てただけば幸いである。