牛の生レバ-の中には腸管出血性大腸菌が検出される場合がある。したがって、生レバーの生食は禁止されている。一方、生卵にはおよそ5000~2万個に一個の割合で1~20cfuのサルモネラ菌が汚染している。しかし、生卵を食べることは禁止されていはない。なぜか?この記事では、その理由について考察してみたい。2つの食中毒菌の食中毒を起こすための発症菌量の違いと、また、これらの発症菌量の違いをもたらす大きな要因としての両者の胃酸に対する抵抗性の違いを説明する。
腸管出血性大腸菌とサルモネラ菌の発症菌数
感染型食中毒菌は基本的に食品と共に体の中に入らないと感染を起こさない。しかし、感染力の強い菌の場合には、トイレや人と人との接触により感染を起こす場合もある。例えば、腸管出血性大腸菌がその例である※。一方、サルモネラ菌の場合は、そのような感染をほとんど起さない。この違いは何か?
※腸管出血性大腸菌による人から人への感染については下記の記事をご覧ください。
空気感染や人から人へうつる場合もある腸管出血性大腸菌
2つの菌の食中毒を起こすための発症菌数の違いが、大きな要因と考えられる。
腸管出血性大腸菌
腸管出血性大腸菌の発症菌数に関しては様々なデータがあるが、FAO and WHO (2011)によれば、代表的なものは以下のとおりである。
- 集団発生に関与した食品のレトロスペクティブな分析、人から人への感染能力、胃の酸性環境での生存を可能にする病原体の酸性条件への耐性に基づき、腸管出血性大腸菌 の感染量は数百細胞以下、さらには摂取した細胞数が10個以下と推定した研究がある
- 他のいくつかの研究 では、25gの食品あたり<2個の細胞でも十分感染を引き起こすことが示されている。これに匹敵する感染量の推定値が CAST (1994)によって提案されている。
- 汚染された乾燥発酵サラミを既知の量で消費した患者について、レトロスペクティブに計算した感染量は、わずか 2 ~ 45 cfuとする研究もある。
- さらに、ある集団発生の際に採取された汚染されたハンバーガーパティには、パティ当たり 0.9 から 4.3 cfu であった。
- 同様に、米国で発生した別の事例では、未調理のハンバーガー・パティに 1 枚あたり 67 から 670 cfu が含まれており、感染量は 700 cfu 未満であることが示唆されている 。しかし、加熱処理されたパティ(消費時)には未調理のものよりも少ない菌が含まれていると考えるのが妥当であるが、実際に摂取された菌の数は不明である。
以上、腸管出血性大腸菌の発症菌数については、数細胞程度であると考えてよさそうである
サルモネラ菌
サルモネラ菌に関してはボランティア実験のデータと、実際の食中毒発生時の食品中のサルモネラ菌数からの2つの推計がある(大腸菌をO157に関しては、症状が重篤で危険なので、ボランティア実験データはない)。
- ボランティア実験:人のボランティアが直接サルモネラ菌を飲み込むボランティア実験では、様々な血清群の感染量は 105 -1010 cfuであることが示されている文献)。サルモネラの教科書などを見ると一般的に発症菌量は105 cfu程度以上と記載している場合が多い。これは、ボランティア実験のデータに基づいていると考えられる。
- 実際の食中毒発生時の食品のサルモネラ菌数からの推計:実際の食中毒発生時のデータから推定した発症菌量は、100 cfu以下( 50%の人が感染し発症するための菌数36cfu)であるとの推計が発表されている(Teunis et al., 2010)。

上記のように、実際の食中毒発生時のデータから推計すると発症菌量は、ボランティア実験から推計した発症菌量よりも、小さくなる。
両者の推計値の違いの主な原因としては次のことが考えられている。
- 集団発生に関与した食品成分が胃酸から菌を保護する役割を果たしている可能性がある。一方、ボランティア実験のほとんどは菌を直接飲み込む実験である。つまり、食品からの保護作用がなく、菌が胃酸で死滅しやすい条件下で実験を行っている。
- 実際の食中毒発生時で患者となる頻度の高い幼児、高齢者、基礎疾患を持った人々などは、健康な成人よりもサルモネラ菌に感染しやすい。しかし、ボランティア実験のほとんどは、健康な成人ボランティアを対象として行われている。

上記のように、サルモネラ菌についてはボランティア実験と実際の食中毒発生時のデータからとのデータ間の推定値が大きく、発症菌数については現時点では不透明な部分も多い。しかし、これらの要素を考慮しても、やはり腸管出血性大腸菌に比べれば、サルモネラ菌の方が発症菌数は高いと考えて良いだろう。
サルモネラ菌と腸管出血性大腸菌の酸への抵抗性
感染型食中毒菌の発症菌量の違いには、感染型食中毒菌の胃酸への抵抗性、小腸で分泌される胆汁酸への抵抗性、腸内環境における腸内細菌叢との競合性、腸管上皮細胞における免疫細胞からの回避力など、様々な要因が関係すると考えられる。しかし、この中でも最も大きな要因と考えられているのが、最初のステップである胃酸の抵抗性である。
以下に、サルモネラ菌と腸管出血性大腸菌の酸に対する抵抗性の違いについてを直接比較したいくつかの論文を紹介する。
液体培地での実験
まずは、大腸菌O157:H7とサルモネラ菌、pH 3・5に調整したトリプチケースソイブロス(tryptic soy broth (TSB))、30℃の生残を調べた論文注)である。
注)この論文では同時にリステリア菌の実験もおこなっているが、本記事では割愛。また、酸への事前適応実験の効果なども調べているが、この記事では割愛。
- サルモネラ菌は、pH 3.5のTSB培地で、 2時間後には7桁以上の菌数の減少を示した。
- 大腸菌O157: H7は8時間後でも、その菌数の減少は3桁にとどまった。
以上の結果から、大腸菌O157は液体培地中でサルモネラ菌よりも酸に対して高い抵抗性を持っていることが示されている。
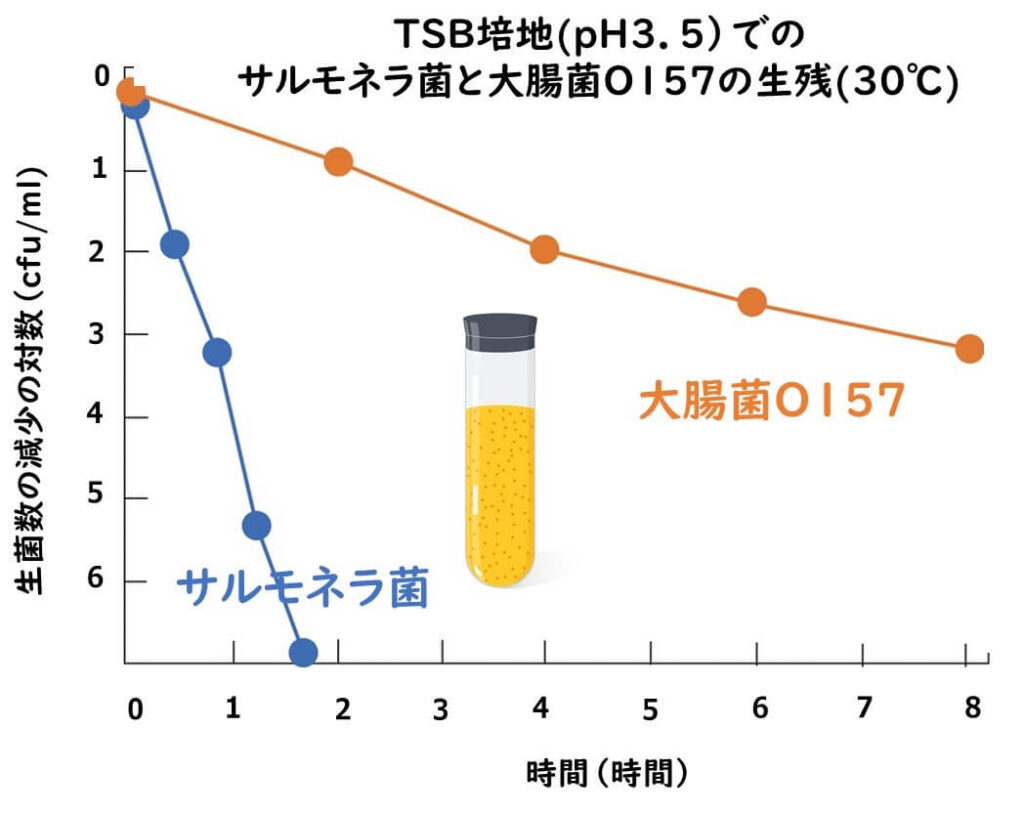
上の図は、下記の論文のデータをもとに作図したものである。
Comparative acid stress response of Listeria monocytogenes, Escherichia coli O157:H7 and Salmonella Typhimurium after habituation at different pH conditions
Letters in Applied Microbiology, 38, 321-326 (2004)
食品での実験
次に牛肉ホモジネートを用いた実験の論文を紹介する。腸管出血性大腸菌O157(STEC)とサルモネラ菌について、無菌の10%牛肉ホモジネートを接種した後、乳酸を5%添加し、生残を調べた注)。
注)この論文では、野生型と抗生物質耐性株の酸に対する抵抗性の比較もしているが、本記事では割愛している。
- サルモネラ菌株のうち、87.9%(33の分離株のうち29)が0〜4分以内に検出限界に達した。
- 大腸菌O157:H7は8分後に検出限界にまで減少した。
これらの結果は、サルモネラ菌は大腸菌O157:H7よりも乳酸を用いた耐酸性が弱いことを示している。
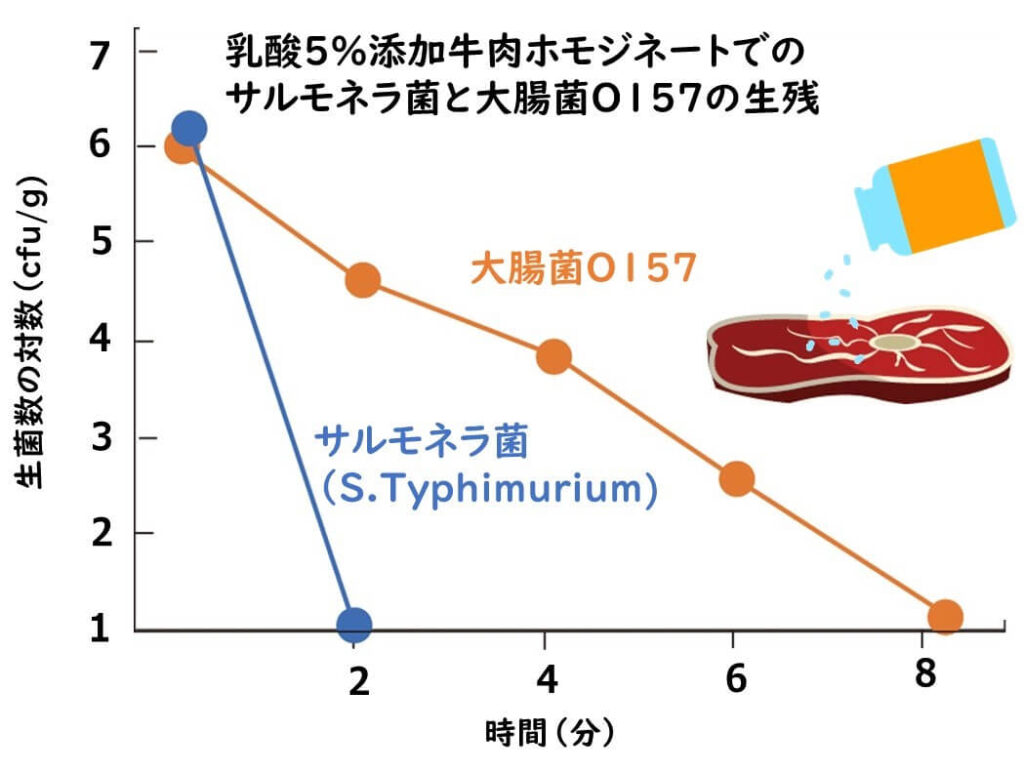
上の図は、下記の論文のデータをもとに作図したものである。
Lactic acid resistance of Shiga toxin-producing Escherichia coli and multidrug-resistant and susceptible Salmonella Typhimurium and Salmonella Newport in meat homogenate
Food Microbiology, 36, 260-266(2013)
胃酸での実験
それでは実際の人間の胃の中を想定した胃酸でのこれら2つの細菌の生残性はどうだろうか?
大腸菌O157とサルモネラ菌を模擬胃酸中での生残性を比較した論文を紹介する。注)。
注)こ論文では、同時にリステリア菌についても実験をおこなっているが、本記事ては割愛している。また、この論文では、低温殺菌および低温未殺菌の防腐剤無添加アップルサイダー(pH3.3-3.5)での生存実験もおこなっているが、この記事では割愛している。
- サルモネラ菌は5分以内に6桁以上減少した。
- 大腸菌O1 57は、180分たっても2桁程度の減少にしか示さなかった。
これらの結果から、大腸菌O157はサルモネラ菌に比べると胃酸のに対して強いことがわかる。
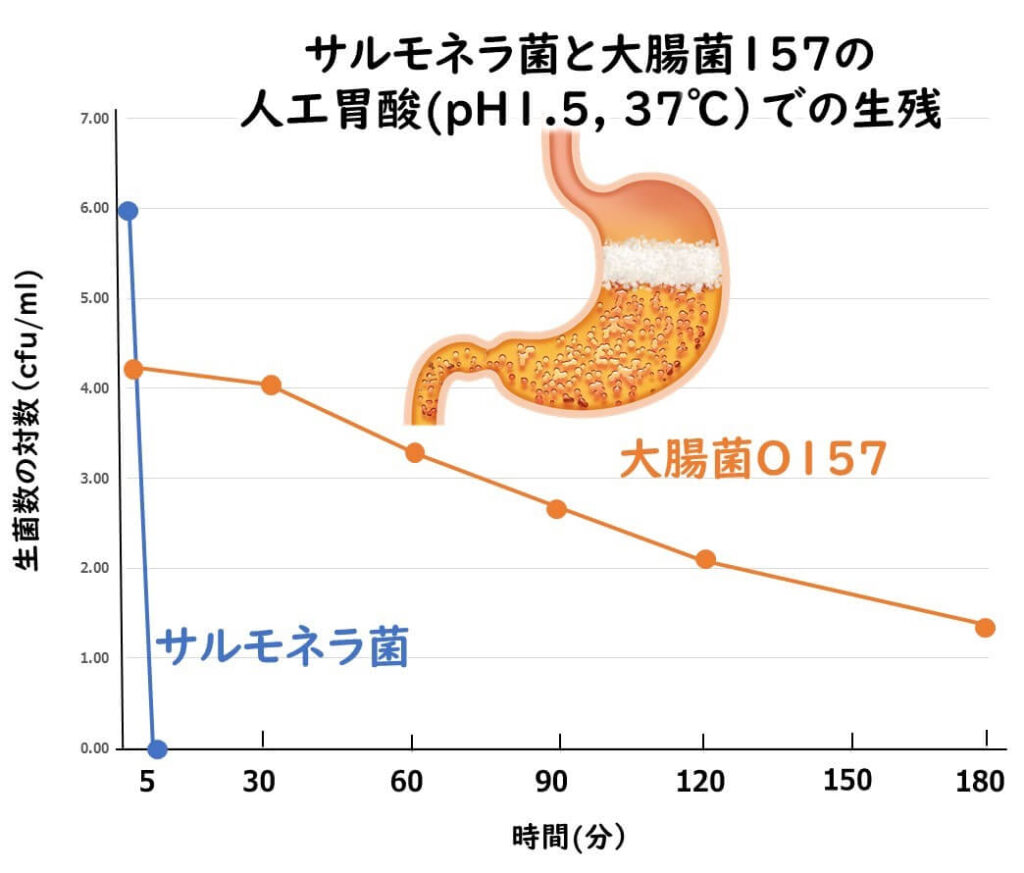
上の図は、下記の論文のデータをもとに作図したものである。
Comparative survival of Salmonella typhimurium DT 104, Listeria monocytogenes, and Escherichia coli O157:H7 in preservative-free apple cider and simulated gastric fluid.
International Journal of Food Microbiology 46 (1999) 263–269
以上、腸管出血性大腸菌はサルモネラ菌に比べると胃酸を含めて、さまざまな酸に対して強い耐性を持っていることがわかる。腸管出血性大腸菌が酸への強い抵抗性を示すメカニズムはまだ詳細にはに解明されされていない。
細菌の酸に対する抵抗性のメカニズムとして、いくつかのアミノ酸デカルボキシラーゼが明らかとなっている。グルタミン酸、アルギニン、およびリジンデカルボキシラーゼなどのアミノ酸デカルボキシラーゼは、それぞれ対象とするアミノ酸を細胞内に取り込んだ上で、細胞内で脱炭酸をする。この際にH+イオンをひとつ消費する。このように、アミノ酸脱炭酸中に細胞質をアルカリ化することによって細菌細胞を保護すると考えられている。この中で腸管出血性大腸菌が用いるグルタミン酸デカルボキシラーゼ(GAD)は、もっとも強力な耐酸性メカニズムの一つと考えられている文献)。
なぜ、腸管出血性大腸菌がいる生レバーは禁止で、サルモネラ菌がいる生卵は禁止されていないの?
以上のように、サルモネラ菌と腸管出血性大腸菌の発症菌量や胃酸への抵抗性の違いを理解した上で、この問いの回答について考えてみよう。
別の記事でも示しているように、生卵にはおよそ5000~2万個に一個の割合で1~20cfuのサルモネラ菌が汚染している。
※サルモネラ菌の汚染とそのリスクについては別記事でまとめてあるのでご覧ください。
生卵は大丈夫なの?
一方、腸管出血性大腸菌は、牛が生きている間に、腸から胆管を経由して肝臓の中に侵入することが研究で明らかになっている。したがって、生レバー食べると、数細胞の大腸菌O157を食べてしまう可能性がある。
生卵を食べる場合には、2万回に一回の割合でサルモネラ菌を直接口の中に入れていることになるが、生卵の生食については現時点では禁止されていない。上述したように、サルモネラ菌の発症菌量は、不透明部分があるにせよ、少なくとも、生卵の割卵直後に含まれている1~20cfuのサルモネラ菌数程度では、感染を起こしにくいと考えにくいからだ注)。
注)卵の割卵後に生卵を室温に放置した場合には、実際には食中毒が起きている。また、生卵をかけた納豆での死亡事例で、民事訴訟で生産者の賠償責任判決も出ている。さらに割卵前の卵を室温で保存した場合には、卵の中のサルモネラ菌の増殖の可能性がある。これらのリスクについては、別記事にまとめているのでご覧ください。
生卵は大丈夫なの?
一方、腸管出血性大腸菌の発症菌量は数細胞なので、仮にレバーに腸管出血性大腸菌が存在していた場合、感染の可能性は否定できない。従って、2012年に厚生労働省牛レバーの生食を禁止された。

結論:腸管出血性大腸菌はサルモネラ菌よりも胃酸に強く、少ない菌数で感染するので、生レバーは禁止
上述したように、腸管出血性大腸菌は、数細胞程度で感染する。したがって生レバーの生食は危険であり、禁止されている。一方、サルモネラ菌は、腸管出血性大腸菌よりも胃酸に対する耐性が弱く、また、発症菌量も大腸菌O157よりも高いと推察することが妥当である。したがって、現時点では生卵の生食は禁止されていない。
法律的には禁止されていないが、サルモネラ菌の発症菌数については現時点で不明瞭な部分もあるので、リスクの観点ではグレーゾーンであることは間違いない。特に免疫力が弱い高齢者、基礎疾患のある人は、生卵の生食は避けたほうがよいであろう。少なくとも割卵してから時間をおいて食べてはいけない。
注)腸管出血性大腸菌の最小発症菌量が非常に少ない理由は、胃酸に対する比較的強い耐性を持つと同時に、その強力な病原性にも起因してる。腸管出血性大腸菌が腸管上皮細胞上で産生するシガトキシンという強力な毒素は、僅かな細胞数でも、腸管壁に重大なダメージを与えることが可能である。この毒素は極微量でも血管内皮細胞に対して致命的な効果を発揮し、重篤な疾患を引き起こす。したがって、腸管出血性大腸菌の感染症は、胃酸に対する耐性と強力な病原性の両方が複合的に作用して発症する可能性が高いと考えられる。